如何修复受损的心脏:斑马鱼心脏再生背后的关键机制被揭示
心血管疾病,如心脏病发作,是全世界死亡的主要原因,这是由于心脏的自我修复能力有限造成的。与人类不同,斑马鱼具有从心脏损伤中恢复的非凡能力。来自Jeroen Bakkers小组(Hubrecht研究所)的研究人员使用斑马鱼来阐明他们的再生成功。他们发现了一种新的机制,可以作为开关推动心肌细胞在再生过程中成熟。重要的是,这种机制在进化上是保守的,因为它对小鼠和人类心肌细胞具有非常相似的作用。
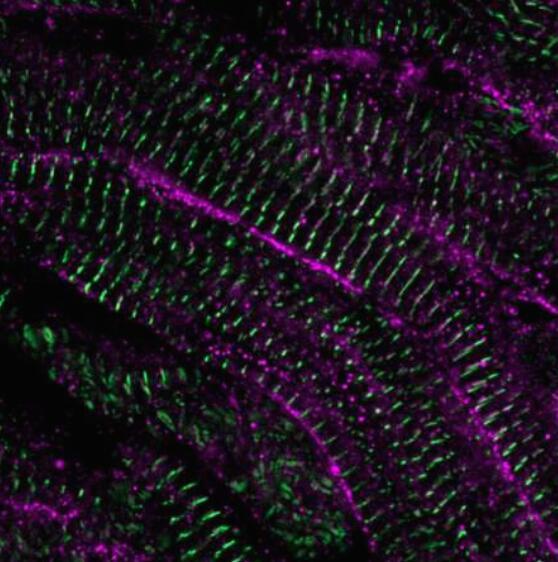
这项研究于18月<>日发表在《科学》杂志上的研究结果显示,研究斑马鱼的自然心脏再生过程并将这些发现应用于人类心肌细胞可能有助于开发针对心血管疾病的新疗法。
据估计,每年有18万人死于心血管疾病。其中许多死亡与心脏病发作有关。在这种情况下,血凝块会阻止向心脏的某些部位供应营养和氧气。结果,心脏阻塞部分的心肌细胞死亡,最终导致心力衰竭。尽管存在控制症状的疗法,但没有治疗方法能够用功能性成熟的心肌细胞替换丢失的组织,从而治愈患者。
斑马鱼作为榜样
与人类不同,斑马鱼等一些物种可以再生心脏。在损伤后90天内,他们完全恢复了心脏功能。幸存的心肌细胞能够分裂并产生更多的细胞。这种独特的功能为斑马鱼的心脏提供了新的组织来源,以取代失去的心肌细胞。以前的研究成功地确定了可以刺激心肌细胞分裂的因素。然而,之后新形成的心肌细胞会发生什么以前没有研究过。
该研究的第一作者Phong Nguyen解释说:“目前尚不清楚这些细胞如何停止分裂并足够成熟,以便它们有助于正常的心脏功能。我们感到困惑的是,在斑马鱼的心脏中,新形成的组织自然成熟并整合到现有的心脏组织中,没有任何问题。
LRRC10 推动成熟
为了详细研究新形成的组织的成熟,研究人员开发了一种技术,将受伤斑马鱼心脏的厚片培养在体外。这使他们能够对心肌细胞中钙的运动进行实时成像。钙进出心肌细胞的调节对于控制心脏收缩很重要,并且可以预测细胞的成熟度。研究小组发现,心肌细胞分裂后,钙的运动会随着时间的推移而改变。
“新分裂细胞中的钙运动最初与胚胎心肌细胞非常相似,但随着时间的推移,心肌细胞呈现出成熟的钙运动类型。我们发现,心脏二元组,一种有助于在心肌细胞内移动钙的结构,特别是其组成部分之一LRRC10,对于决定心肌细胞是分裂还是成熟进展至关重要。缺乏LRRC10的心肌细胞继续分裂并保持不成熟,“Nguyen说。
从鱼到人
在Nguyen和他的同事确定了LRRC10在阻止细胞分裂和启动斑马鱼心肌细胞成熟方面的重要性之后,他们继续测试他们的发现是否可以转化为哺乳动物。为此,他们在小鼠和实验室培养的人心肌细胞中诱导LRRC10的表达。
引人注目的是,LRRC10改变了钙的处理,减少了细胞分裂,并以与斑马鱼心脏中观察到的类似方式增加了这些细胞的成熟。Nguyen说:“看到从斑马鱼身上学到的经验教训是可以翻译的,这为LRRC10在患者新疗法中的使用开辟了新的可能性,这令人兴奋。
临床影响
发表在《科学》杂志上的研究结果显示,LRRC10有可能通过控制心肌细胞的钙处理来进一步推动心肌细胞的成熟。这可以帮助那些试图通过将实验室培养的心肌细胞移植到受损心脏中来解决哺乳动物心脏缺乏再生能力的科学家。尽管这种潜在的疗法很有希望,但结果表明,这些实验室培养的细胞仍未成熟,无法与心脏的其他部分正常沟通,导致称为心律失常的异常收缩。
“虽然需要更多的研究来精确定义这些实验室培养的心肌细胞在用LRRC10治疗时的成熟程度,但成熟度的增加可能会改善移植后的整合,”该研究的最后一作者Jeroen Bakkers说。
“此外,目前的心脏病模型通常基于未成熟的实验室培养的心肌细胞。在实验室中发现的90%有前途的候选药物未能进入临床,这些细胞的不成熟可能是这种低成功率的一个因素。我们的结果表明,LRRC10也可以提高这些模型的相关性。
因此,LRRC10可以为产生实验室培养的心肌细胞做出重要贡献,这些心肌细胞更准确地代表典型的成年人心脏,从而提高成功开发心血管疾病新疗法的机会。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
安徽淮南地区的长安汽车经销商近期对2025款启源Q05车型的市场策略进行了调整,以进一步吸引消费者。作为长安汽...浏览全文>>
-
近年来,豪华SUV市场持续升温,而作为大众旗下的高端品牌,途锐凭借其卓越的性能与豪华配置,一直深受消费者的...浏览全文>>
-
在新能源汽车市场中,一汽-大众ID 4 CROZZ凭借其出色的性价比和丰富的配置吸引了众多消费者的关注。作为一款...浏览全文>>
-
近年来,随着国内汽车市场的快速发展,越来越多的消费者开始关注性价比高的小型车。QQ多米作为一款备受关注的...浏览全文>>
-
在当今的汽车市场中,选择一款高性价比的车型是许多消费者的重要考量。对于追求品质与经济平衡的购车者来说,...浏览全文>>
-
阜阳地区消费者对上汽大众途岳的关注度一直很高,尤其是2025款途岳的上市更是引发了广泛关注。作为一款紧凑型S...浏览全文>>
-
天津滨海长安猎手K50作为一款备受关注的车型,在市场上拥有较高的关注度。这款车型以其出色的性能和合理的价格...浏览全文>>
-
近年来,随着新能源汽车的普及,插电混动车型因其兼顾燃油经济性和驾驶性能的特点,受到了越来越多消费者的青...浏览全文>>
-
途观X作为上汽大众旗下的高端轿跑SUV车型,凭借其时尚动感的外观设计和丰富的科技配置,在市场上一直备受关注...浏览全文>>
-
在选择SUV车型时,上汽大众途昂凭借其宽敞的空间和强大的性能成为不少消费者的首选。对于蚌埠地区的消费者来说...浏览全文>>
- 天津滨海长安猎手K50多少钱 2025款落地价,最低售价18.29万起,赶紧行动
- 天津滨海ID.4 CROZZ 2025新款价格,买车省钱秘籍
- 安徽淮南途昂X多少钱?性价比超高的选车秘籍
- 福特领睿试驾,开启完美驾驭之旅
- 比亚迪海豹05DM-i试驾预约流程
- 凯迪拉克CT5预约试驾,从预约到试驾的完美旅程
- 滁州途观X落地价,各配置车型售价全知晓
- 极狐 阿尔法T6试驾,开启完美驾驭之旅
- 长安欧尚520试驾操作指南
- QQ多米试驾需要注意什么
- 长安Lumin试驾,感受豪华与科技的完美融合
- 安庆长安猎手K50最新价格2025款与配置的完美平衡
- 池州迈腾GTE最新价格2022款全解,买车必看的省钱秘籍
- 安徽亳州ID.6 X多少钱?购车全攻略来袭
- 五菱雪宝试驾,开启豪华驾驶之旅
- 马自达EZ-6预约试驾,新手必看的详细流程
- 安徽亳州T-ROC探歌落地价实惠,配置丰富,不容错过
- 滁州高尔夫GTI价格大揭秘,买车前必看
- 东莞威然落地价,最低售价22.99万起优惠不等人
- 试驾王牌M7,体验豪华驾乘的乐趣
